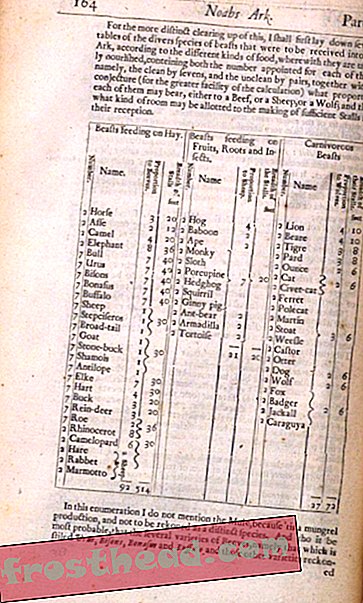
Um recife de corais leva milhares de anos para ser construído, mas pode desaparecer em um instante.
Conteúdo Relacionado
- Corais de águas profundas brilham por suas vidas
- O último evento de branqueamento pode ter acabado, mas os recifes ainda estão em perigo
O culpado geralmente é o branqueamento de corais, uma doença exacerbada pelo aquecimento das águas que hoje ameaça os recifes em todo o mundo. O pior evento de branqueamento registrado atingiu o Pacífico Sul entre 2014 e 2016, quando o aumento da temperatura do oceano, seguido de um súbito afluxo de águas quentes de El Niño, traumatizou a Grande Barreira de Corais. Em apenas uma estação, o branqueamento dizimou quase um quarto do vasto ecossistema, que uma vez se espalhou por quase 150.000 milhas quadradas através do Mar de Coral.
“Por pior que tenha sido, esse evento de branqueamento foi um alerta”, diz Rachel Levin, uma bióloga molecular que recentemente propôs uma técnica ousada para salvar esses ecossistemas essenciais. Sua idéia, publicada na revista Frontiers in Microbiology, é simples: ao invés de encontrar simbiontes saudáveis para repovoar os corais branqueados na natureza, desenvolva-os no laboratório. Dado que isso exigiria adulteração da natureza de forma significativa, a proposta é susceptível de agitar águas polêmicas.
Mas Levin argumenta que com o tempo se esgotando para os recifes em todo o mundo, o valor potencial pode valer a pena o risco.
Levin estudou farmacologia do câncer na graduação, mas ficou fascinado com as ameaças que a vida aquática enfrenta enquanto se interessa por cursos de ciências marinhas. Ela ficou impressionada com o fato de que, diferentemente da pesquisa sobre doenças humanas, havia muito menos pesquisadores lutando para restaurar a saúde dos oceanos. Depois que ela se formou, ela se mudou da Califórnia para Sydney, na Austrália, para obter um Ph.D. no Centro de Bioinovação Marinha da Universidade de New South Wales, com a esperança de aplicar seus conhecimentos em pesquisa de doenças humanas em corais.
Na medicina, muitas vezes leva a ameaça de uma doença grave para os pesquisadores tentarem um tratamento novo e controverso (ou seja, fundir dois óvulos saudáveis das mulheres com o esperma de um homem para formar um “bebê com três filhos”). O mesmo se aplica à ciência ambiental - até certo ponto. "Como uma doença terrível [em] seres humanos, quando as pessoas percebem o quão terrível a situação está se tornando pesquisadores começam a tentar propor muito mais", diz Levin. Quando se trata de salvar o meio ambiente, no entanto, há menos defensores dispostos a implementar técnicas arriscadas e inovadoras.
Quando se trata de recifes - regiões marinhas cruciais que abrigam uma quantidade surpreendente de diversidade, bem como protegem as massas de terra de tempestades, enchentes e erosão -, a hesitação pode ser fatal.
O branqueamento de corais é frequentemente apresentado como a morte de corais, o que é um pouco enganador. Na verdade, é o colapso da união simbiótica que permite que um coral prospere. O próprio animal de coral é como um construtor de edifícios que constrói os andaimes de um complexo de apartamentos altos. O desenvolvedor aluga cada um dos bilhões de quartos para micróbios fotossintéticos unicelulares chamados Symbiodinium.
Mas neste caso, em troca de um lugar seguro para viver, Symbiodinium faz comida para o coral usando a fotossíntese. Um coral branqueado, ao contrário, é como um prédio abandonado. Sem inquilinos para fazer suas refeições, o coral acaba morrendo.
Embora o branqueamento possa ser mortal, na verdade é uma estratégia evolutiva inteligente do coral. Espera-se que os Symbiodinium mantenham o seu fim do negócio. Mas quando a água fica muito quente, eles param a fotossíntese. Quando essa comida fica escassa, o coral envia um aviso de despejo. "É como ter um inquilino ruim - você vai se livrar do que tem e ver se consegue encontrar melhor", diz Levin.
Mas à medida que os oceanos continuam a aquecer, é cada vez mais difícil encontrar bons inquilinos. Isso significa que despejos podem ser arriscados. Em um oceano em aquecimento, o animal de coral pode morrer antes de encontrar locatários melhores - um cenário que dizimou os ecossistemas de recifes ao redor do planeta.
Levin queria resolver esse problema, criando uma receita direta para construir um super-simbionte que pudesse repovoar os corais branqueados e ajudá-los a persistir através da mudança climática - essencialmente, os inquilinos perfeitos. Mas ela teve que começar pequena. Na época, "havia muitos buracos e lacunas que nos impediam de avançar", diz ela. "Tudo o que eu queria fazer era mostrar que podíamos manipular geneticamente [ Symbiodinium ]".
Mesmo isso seria uma tarefa difícil. O primeiro desafio foi que, apesar de ser um organismo unicelular, o Symbiodinium tem um genoma pesado. Normalmente, os organismos simbióticos têm genomas simplificados, já que dependem de seus hospedeiros para a maioria de suas necessidades. No entanto, enquanto outras espécies têm genomas de cerca de 2 milhões de pares de bases, o genoma do Symbiodinium é 3 ordens de magnitude maior.
"Eles são gigantescos", diz Levin. De fato, todo o genoma humano é apenas um pouco menos de 3 vezes maior que o do Symbiodinium .
Mesmo depois que os avanços no sequenciamento do DNA tornaram possível decifrar esses genomas, os cientistas ainda não tinham ideia do que eram 80% dos genes. "Precisávamos recuar e juntar o gene que estava fazendo o que neste organismo", diz Levin. Um membro de um grupo de fitoplâncton chamado dinoflagelados, Symbiodinium são incrivelmente diversos. Levin voltou sua atenção para dois tipos principais de Symbiodinium que ela poderia cultivar em seu laboratório.
A primeira cepa, como a maioria dos Symbiodinium, era vulnerável às altas temperaturas que causam o branqueamento de corais. Aumente o dial de aquecimento em alguns entalhes, e esse bicho era torrado. Mas a outra linhagem, que havia sido isolada dos raros corais que vivem nos ambientes mais quentes, parecia ser impermeável ao calor. Se ela pudesse descobrir como essas duas variedades usavam seus genes durante as condições de branqueamento, ela poderia encontrar as chaves genéticas para criar uma nova super-estirpe.
Quando Levin aumentou o calor, ela viu que o resistente Symbiodinium aumentava sua produção de antioxidantes e proteínas de choque térmico, que ajudam a reparar os danos celulares causados pelo calor. Sem surpresa, o Symbiodinium normal não. Levin então voltou sua atenção para descobrir uma maneira de inserir mais cópias desses genes cruciais tolerantes ao calor no Symbiodinium mais fraco, criando assim uma cepa adaptada para viver com os corais das regiões temperadas - mas com as ferramentas para sobreviver aquecendo os oceanos.
Obter novo DNA em uma célula dinoflagelada não é tarefa fácil. Embora pequenas, essas células são protegidas por placas blindadas, duas membranas celulares e uma parede celular. "Você pode passar, se você empurrar com força suficiente", diz Levin. Mas, novamente, você pode acabar matando as células. Então Levin solicitou ajuda de um improvável colaborador: um vírus. Afinal, os vírus "evoluíram para serem capazes de colocar seus genes no genoma do hospedeiro - é assim que eles sobrevivem e se reproduzem", diz ela.
Levin isolou um vírus que infectou Symbiodinium, e o alterou molecularmente para não mais matar as células. Em vez disso, ela projetou para ser um sistema de entrega benigna para aqueles genes tolerantes ao calor. Em seu trabalho, Levin argumenta que a carga do vírus poderia usar CRISPR, a técnica inovadora de edição de genes que depende de um processo natural usado por bactérias, para cortar e colar esses genes extras em uma região do genoma do Symbiodinium, onde eles seriam altamente expresso.
Parece bastante simples. Mas mexer com um ecossistema vivo nunca é simples, diz Dustin Kemp, professor de biologia na Universidade do Alabama, em Birmingham, que estuda os impactos ecológicos da mudança climática nos recifes de corais. “Sou muito a favor dessas soluções para conservar e ajudar geneticamente”, diz Kemp. Mas “reconstruir recifes que levaram milhares de anos para se formar será uma tarefa muito difícil”.
Considerando a diversidade impressionante das cepas de Symbiodinium que vivem dentro de apenas uma espécie de coral, mesmo se houvesse um sistema robusto de modificação genética, Kemp se pergunta se seria possível projetar super- Symbiodinium o suficiente para restaurar essa diversidade. “Se você cortar uma floresta antiga e depois plantar alguns pinheiros, isso realmente está salvando ou reconstruindo a floresta?”, Pergunta Kemp, que não estava envolvido no estudo.
Mas Kemp concorda que os recifes estão morrendo em um ritmo alarmante, rápido demais para que a evolução natural da Symbiodinium seja mantida . “Se os corais estivessem evoluindo rapidamente para lidar com [aquecer as águas], você pensaria que já teríamos visto isso”, diz ele.
Thomas Mock, um microbiologista marinho da Universidade de East Anglia, no Reino Unido, e pioneiro na modificação genética do fitoplâncton, também aponta que a biologia de dinoflagelados ainda está amplamente envolta em mistério. "Para mim isso está brincando", diz ele. “Mas é assim que tudo começa normalmente. Argumento provocativo é sempre bom - é muito desafiador, mas vamos começar em algum lugar e ver o que podemos alcançar. ”Recentemente, CSIRO, a divisão científica do governo australiano, anunciou que financiará laboratórios para continuar pesquisando modificações genéticas em simbiontes de corais.
Quando se trata de saúde humana - por exemplo, proteger humanos contra doenças devastadoras como malária ou zika -, os cientistas estão dispostos a tentar técnicas mais drásticas, como a liberação de mosquitos geneticamente programados para transmitir genes letais. As modificações genéticas necessárias para salvar os corais, argumenta Levin, não seriam tão extremas. Ela acrescenta que muito mais testes de laboratório controlados são necessários antes que Symbiodinium geneticamente modificado possa ser liberado no meio ambiente para repovoar os recifes de corais.
"Quando estamos falando de 'engenharia genética', não estamos alterando significativamente essas espécies", diz ela. “Não estamos fazendo coisas imensamente mutantes. Tudo o que estamos tentando fazer é dar a eles uma cópia extra de um gene que eles já têm para ajudá-los ... não estamos tentando ser cientistas loucos. ”